Съдържание
Процентната маса определя процента на всеки елемент, който образува химично съединение. За да намерите тази стойност, ще ви е необходима моларната маса на съставните елементи в грамове / молове или броят на грамовете, използвани за създаване на разтвора. Процентната маса може да бъде изчислена по прост начин, като се използва основна формула, която разделя масата на елемента (или разтвореното вещество) на масата на съединението (или разтвора).
Стъпки
Метод 1 от 2: Намиране на процентната маса с дадени маси
- Дефинирайте уравнението за процентната маса на съединението. Основната формула за съединение е: процентна маса = () x 100. Трябва да умножите резултата по 100 в края, за да изразите стойностите като проценти.
- Масата на химично съединение, от което се интересувате, е масата, дадена в задачата. Ако тази стойност не е предоставена, вижте следния метод и научете как да намерите процентната маса, когато масата не е дадена.
- Общата маса на съединението се изчислява чрез добавяне на масите на всички елементи, използвани за създаване на съединението или разтвора.
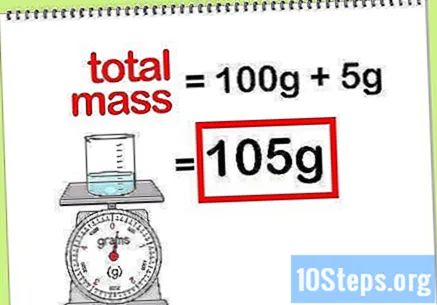
Изчислете общата маса на съединението. Когато знаете стойността на масата на всички добавени елементи или съединения, просто трябва да ги добавите, за да изчислите масата на съединението или крайния разтвор. Тази стойност ще бъде знаменателят при изчисляването на процентната маса.- Например: Каква е процентната маса на 5 g натриев хидроксид, разтворен в 100 g вода?
- Общата маса на съединението е количеството натриев пероксид плюс количеството вода: 100 g + 5 g, общо маса 105 g.

Идентифицирайте масата на въпросния химикал. Когато трябва да намерите процентна маса, проблемът иска да намерите масата на конкретен елемент (въпросният елемент) като процент от общата маса на всички елементи. Обърнете внимание на масата на въпросния елемент. Тази стойност ще бъде числителят при изчисляването на процентната маса.- Например, масата на елемента е 5 g натриев хидроксид.
- Заменете променливите във формулата за процентно тегло. След определяне на стойностите за всяка променлива ги заменете в уравнението.
- Например: процентна маса = () x 100 = () x 100.

Изчислете процентната маса. Сега, когато се формира уравнението, просто го решете, за да изчислите процентната маса. Разделете масата на елемента на общата маса на съединението и умножете по 100. Резултатът ще бъде процентната маса на химичния елемент.- Например: () x 100 = 0,04761 x 100 = 4,751%. По този начин процентното тегло на 5 g натриев хидроксид, разтворен в 100 g вода, е 4.751%.
Метод 2 от 2: Намиране на процентната маса с непосочени маси
- Дефинирайте уравнението за процентната маса на съединението. Основната формула за процентната маса на съединението е: процентна маса = () x 100. Трябва да умножите резултата по 100 в края, за да изразите стойностите като проценти.
- Когато не знаете стойностите на масата, можете да намерите процентната маса на елемент от съединението, като използвате моларната маса.
- Например: Каква е процентната маса на водорода във водна молекула?.
Напиши химична формула. Ако химичните формули за всяко съединение не са предоставени, ще трябва да ги запишете. В противен случай преминете към Стъпка „Намиране на масата на всеки елемент“.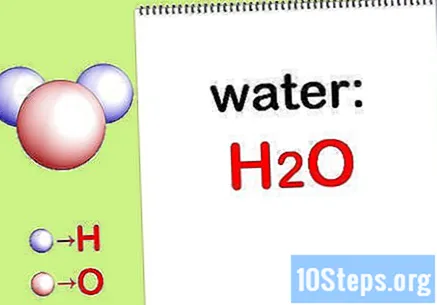
- Например напишете химическата формула за вода: H2НА.
Намерете масата на всеки елемент в съединението. Потърсете молекулното тегло на всеки елемент от химичните формули, като се обърнете към периодичната таблица. Обикновено масата на даден елемент може да бъде намерена под символа на химичния елемент. Обърнете внимание на масите на всеки елемент от съединението.
- Например молекулната маса на кислорода е 15,9994, а тази на водорода е 1,0079.
Умножете масите по моларното съотношение. Идентифицирайте колко мола на всеки елемент има в химичното съединение. Броят на бенките се дава от записания номер на съединението. Умножете молекулната маса на всеки елемент по моларното съотношение.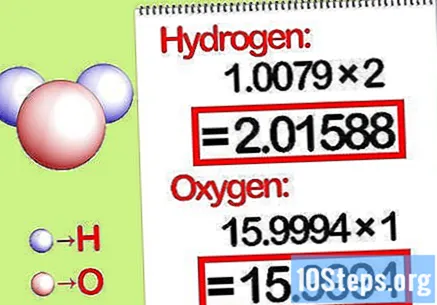
- Например, моларното съотношение на водород към кислород във вода е 2: 1. Следователно, умножете молекулното тегло на водорода по два (1.00794 X 2 = 2.01588) и оставете молекулното тегло на кислорода такова, каквото е (15.9994).
Изчислете общата маса на съединението. Добавете общата маса на всички елементи на съединението. Използвайки масите, изчислени от моларното съотношение, е възможно да се изчисли общата маса на съединението. Това число ще бъде знаменателят на уравнението на процентната маса.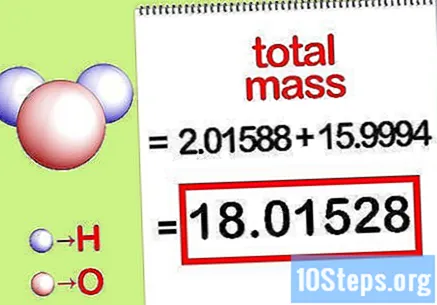
- Например, добавете 2,01588 g / mol (масата на два мола водородни атоми) с 15,9994 g / mol (масата на един мол кислороден атом) и получете 18,01528 g / mol.
Идентифицирайте масата на въпросния елемент. Когато трябва да намерите процентна маса, проблемът иска да намерите масата на определен елемент в дадено съединение като процент от общата маса на всички елементи. Идентифицирайте масата на въпросния елемент и го запишете. Това е стойността на масата, изчислена с помощта на моларното съотношение. Тази стойност е числителят на уравнението на процентната маса.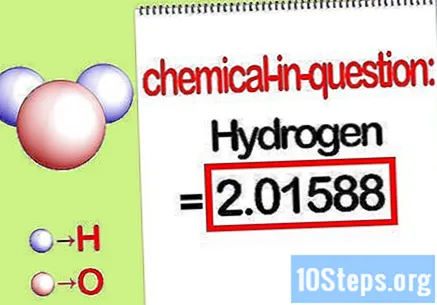
- Например, водородната маса на съединението е 2,01588 g / mol (масата на два мола водородни атоми).
- Заменете променливите във формулата за процентно тегло. След определяне на стойностите за всяка променлива ги заменете в уравнението, дефинирано в първата стъпка: процентна маса = () x 100.
- Например: процентна маса = () x 100 = () x 100.
Изчислете процентната маса. Сега, когато се формира уравнението, просто го решете, за да изчислите процентната маса. Разделете масата на елемента на общата маса на съединението и умножете по 100. Резултатът ще бъде процентната маса на химичния елемент.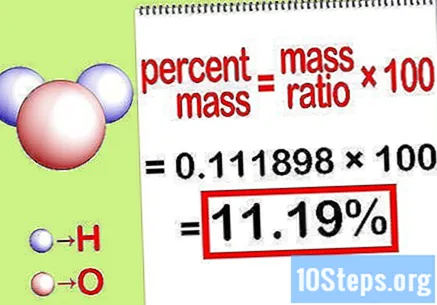
- Например, процентна маса = () x 100 = 0,111189 x 100 = 11,18%. По този начин процентната маса на водородните атоми във водна молекула е 11,18%.