Съдържание
Атомният номер съответства на броя на протоните в ядрото на отделен атом на елемент. Тази стойност не се променя; следователно можете да го използвате, за да откриете други характеристики на изотопа, като например броя на неутроните.
Стъпки
Част 1 от 2: Намиране на атомното число
Намерете копие на периодичната таблица. Щракнете тук, ако нямате такъв. Всеки елемент има свой собствен атомен номер; по този начин няма преки пътища за изучаване на съдържанието. Използвайте копие на таблицата или се опитайте да го запомните.
- В повечето книги по химия таблицата е отпечатана на задната корица.

Намерете елемента, който изучавате, в таблицата. Повечето таблици включват пълното име на елементите, както и техните символи (Hg за живак например). Ако не можете да намерите това, което търсите, влезте в мрежата и направете търсене с термините „химичен символ“ и името на елемента.
Намерете атомния номер на елемента. Обикновено е в горния ляв или десен ъгъл на къщата на елемента, но може да дойде и на други места. В допълнение, това винаги е цяло число.- Ако числото включва десетична точка, това вероятно показва атомната маса.
Потвърдете информацията според елементите наблизо. Периодичната таблица е организирана според реда на атомните числа. Ако вашият изотопен номер е "33", например, елементът отляво ще бъде "32", а този отдясно ще бъде "34". В този случай това е така, защото гледате атомния номер.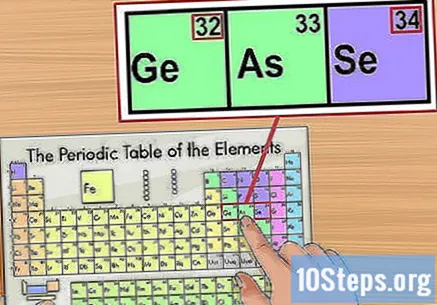
- Има скок между елементите "56" (барий) и "88" (радио). Изотопите, които съответстват на този диапазон, са в двата реда под таблицата. Те са разделени само по този начин, така че масата да не е твърде голяма.
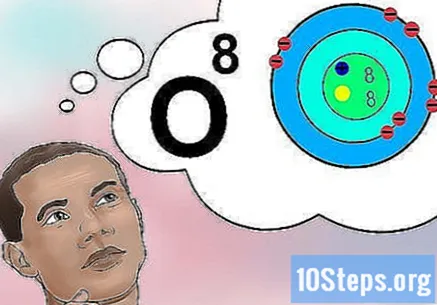
Разберете какво означава атомното число. Атомният номер има проста дефиниция: количеството протони в атом на елемента. Това количество протони от своя страна определя общия електрически заряд на ядрото - което следователно определя колко електрони може да зареди атомът. Тъй като електроните са отговорни за почти всички химични взаимодействия, атомният номер косвено влияе върху физико-химичните свойства на елемента.- С други думи, всеки атом с осем протона съответства на кислороден атом. Два кислородни атома могат да имат различен брой неутрони или (ако единият е йон) или електрони, но те винаги ще имат по осем протона.
Част 2 от 2: Откриване на по-важна информация
Определете атомното тегло. Обикновено той идва под името на елемента в периодичната таблица и има два или три знака след десетичната запетая. Атомното тегло съответства на средната маса на атомите на даден елемент, представящ как се намира в природата. Измерва се в "атомни единици за маса" ("u" или "u.m.a").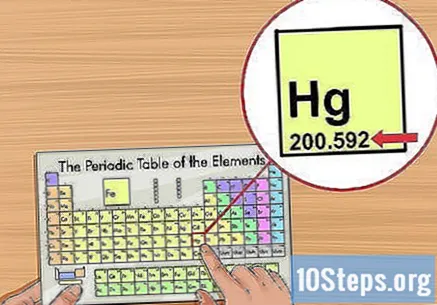
- Много учени предпочитат да използват термина „атомна маса“ вместо тегло.
Разберете атомната маса. Концепцията за атомната маса е много подобна на тази за теглото. Разликата е, че теглото показва средната маса на всеки атом в елемента, а не на конкретен атом. Например: грам желязо съдържа няколко атома с различна маса; теглото показва тяхната "относителна маса". Ако изучавате един атом на елемента, просто трябва да знаете неговата специфична маса.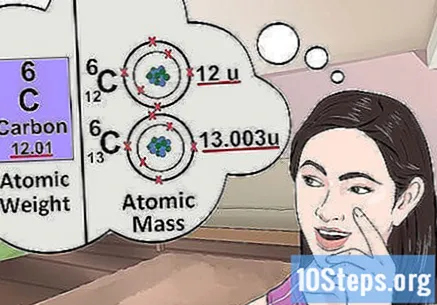
- Като цяло, химичните проблеми, включващи само атоми, вече информират атомното масово число. Просто трябва да разберете концепцията, за да не бъдете изненадани, когато видите различна стойност.
Закръглете масовото число. Масовото число съответства на общото количество протони и неутрони в атом на елемента. Не е трудно да се изчисли: просто вземете атомната маса, отпечатана на периодичната таблица, и я закръглете до най-близката цяла стойност.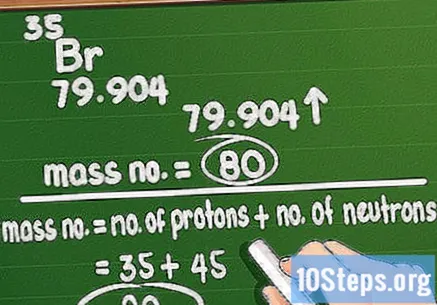
- Това работи, тъй като количествата неутрони и протони са много близки до 1 u.m.a., докато това на електроните е много близо до нула. Атомната маса включва точни изчисления за определяне на десетичната стойност, но единствените данни, които имат значение, са цели числа, които ви казват колко протони и неутрони има.
- Не забравяйте, че ако използвате атомна маса, ще се забъркате с теглото на конкретен атом в даден елемент. Бромната проба например има атомна маса 79 или 81.
Изчислете броя на неутроните. Вече знаете, че атомният номер е равен на броя на протоните и че масовото число е равно на сумата от броя на протоните и неутроните. За да определите количеството неутрони в даден елемент, просто извадете атомното число от тази обща маса. Няколко примера:
- Хелиевият атом (He) има масово число 4 и атомен номер 2. Следователно 4 - 2 = 2 неутрона.
- Проба от сребро (Ag) има средно масово число 108 (според периодичната таблица) и атомно число 47. Средно всеки атом в пробата има 108 - 47 = 61 неутрона.
Разберете изотопите. Изотопът е специфична форма на елемент, който съдържа редица неутрони. Ако проблемът, който искате да разрешите, носи нещо като "бор-10" или "В", това е така, защото говорите за елементите на бор с масовото число 10. Използвайте тази стойност, а не "нормалните" стойности на бор.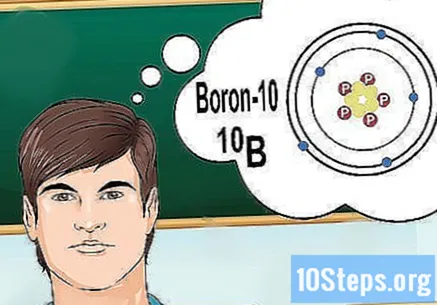
- Атомният номер на изотопите никога не се променя. Всеки изотоп на елемент има еднакъв брой протони.
Съвети
- Атомното тегло на някои по-тежки елементи е в скоби или квадратни скоби. Това означава, че това тегло е точната маса на най-стабилния изотоп, а не средно няколко изотопа. И накрая, това не засяга атомния номер на елемента.