
Съдържание
- етапи
- Метод 1 Балансиране на уравнение по метода на проба и грешка
- Метод 2 Изравнете уравнение по алгебраичния метод
В химията уравнение установява какво се е случило по време на химическа реакция. Вляво от уравнението поставяме реагентите, които са били използвани за експеримента, а отдясно продуктите, получени по време на експеримента. Според принципа на запазване на масата (Lavoisier) по време на химическа реакция, никой атом не изчезва, нито един не се създава, те се комбинират по различен начин. В обобщение, трябва да имате същия брой дотоми на всеки елемент отдясно, както вляво от уравнението. Ето защо уравнението на баланса винаги трябва да бъде балансирано.
етапи
Метод 1 Балансиране на уравнение по метода на проба и грешка
-
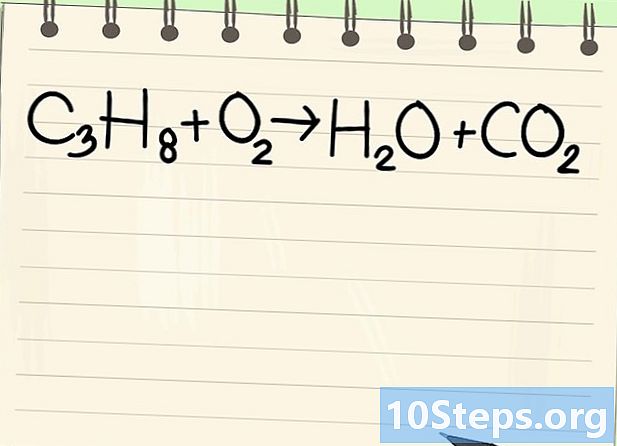
Забележете уравнението на баланса. Ще разгледаме следното уравнение:- C3Н8 + О2 -> H2O + CO2
- Това е уравнението на изгарянето на пропан (С3Н8) в кислорода: получават се вода и въглероден диоксид.
-
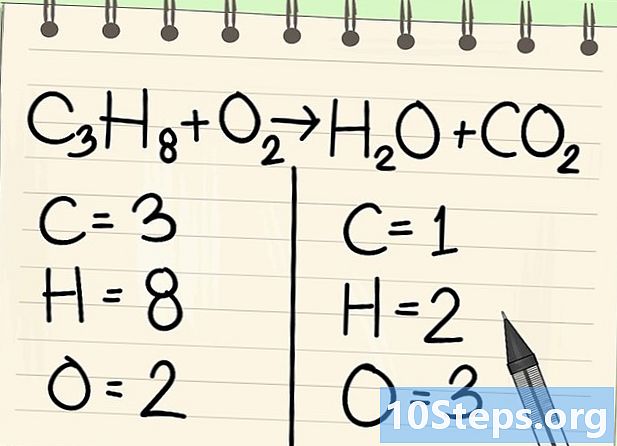
Пребройте атомите. Въведете броя на датите на всеки елемент от едната страна на уравнението, след това от другата. За това вземете предвид индексите, ако няма такива, индексът е 1.- Отляво има 3 въглеродни атома, 8 водорода и 2 кислорода.
- Вдясно има 1 атом въглерод, 2 водород и 3 кислород.
-
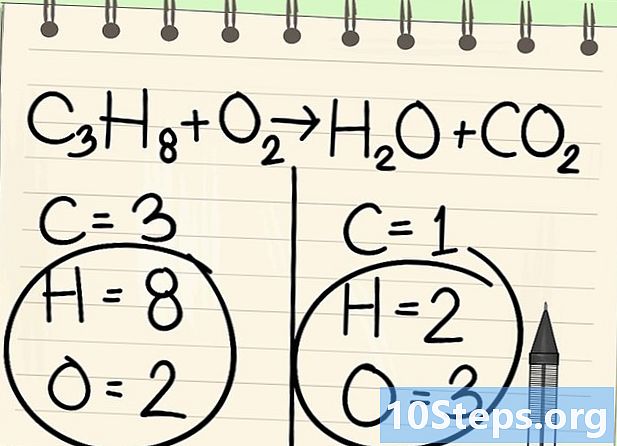
Оставете за миг настрана водорода и кислорода. -

Започнете да балансирате с правилния елемент. Винаги започваме с този в молекула преди и след реакцията. Ако са няколко, вземете тази, която е едновалентна в една от молекулите. Тук започваме с въглеродните атоми. -

Балансирайте въглеродните атоми. Добавете отдясно коефициент към молекулата на въглеродния диоксид (CO2), в който въглеродният латом е сам. Ще сложим 3, за да получим 3-те леви атома.- C3Н8 + О2 -> H2О + 3CO2
- По този начин имаме 3 въглеродни атома вдясно благодарение на коефициента (3CO2) и 3 въглеродни атома вляво благодарение на индекса (C3Н8).
- В уравнение можете да поставите всички желани коефициенти, но не можете да докоснете уликите.
-
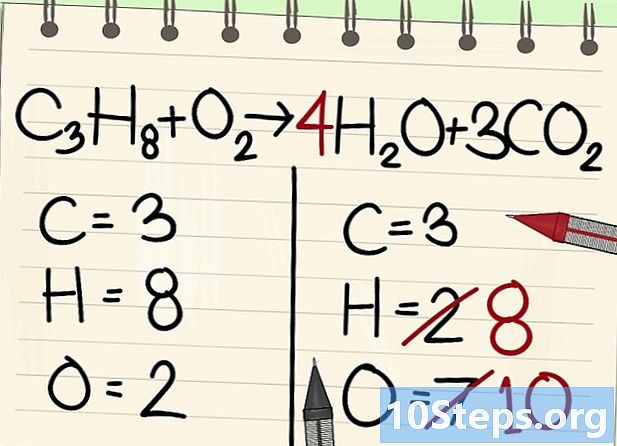
Балансирайте водородните атоми. Тъй като имате 8 вляво от уравнението, имате нужда от толкова дясно.- C3Н8 + О2 --> 4Н2O + 3CO2
- Отдясно ще поставите коефициент 4, защото водородът е двувалентен във водната молекула: индексът 2 показва, че два водородни атома са свързани.
- За да получите броя на водородните атоми вдясно, умножавате коефициента 4 с индекса 2 или 8 атома.
- Що се отнася до атомите на кислорода, вдясно, сега има 6 от едната страна, идващи от трите молекули на 3CO2 (3 х 2 = 6 атома) и 4 от 4-те молекули на 4Н20 (4 х 1 = 4 атома), т.е. общо 10 атома кислород.
-
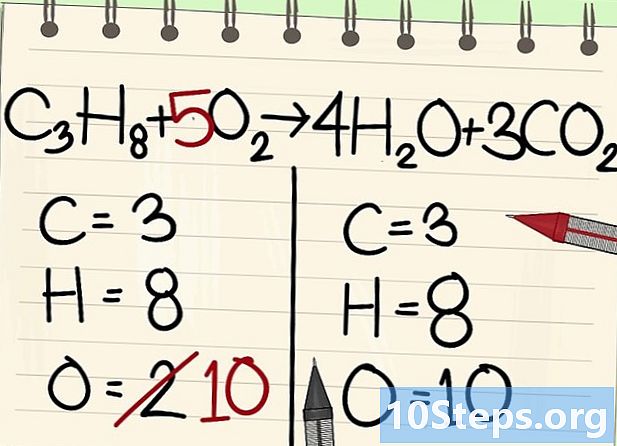
Балансирайте атомите на кислорода.- Поради баланса на въглерода и водорода броят на кислородните атоми не е еднакъв от двете страни на уравнението. По-рано видяхме, че вдясно има 10 атома кислород (4 от молекулите на водата и 6 от молекулите на въглеродния диоксид). Отляво има само 2 (от О2).
- За да балансирате кислорода, добавете коефициент 5 към лявата молекула на кислорода: имате 10 атома кислород отляво, а другият отдясно.
- C3Н8 + 5О2 -> 4Н2O + 3CO2
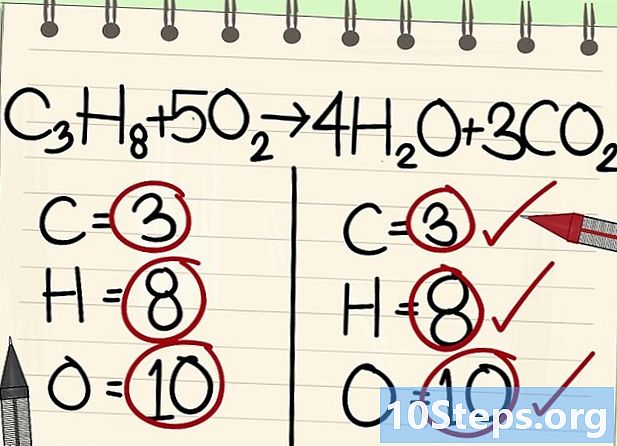
- Всички атоми (въглерод, водород и кислород) са балансирани: уравнението ви е балансирано.
Метод 2 Изравнете уравнение по алгебраичния метод
-

Напишете уравнението, за да балансирате. Задайте на всяка молекула буквален коефициент. Ще им се обадим има, б, в и г. -
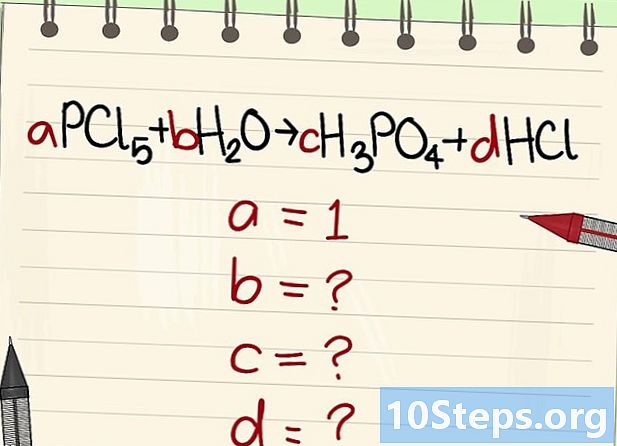
Намерете стойността на другите буквални коефициенти. Ще го попитаме има = 1. -

Намерете връзките между тези коефициенти. Поглеждайки вляво (реагенти) и вдясно (продукти), установете връзките между тези различни коефициенти.- Вземете следното уравнение: aPCl5 + bH2O = cH3PO4 + dHCl. Беше заявено, че a = 1, което означава, че c = a, d = 5a и 2b = 3c + d. Извършени изчисления, c = 1, d = 5 и b = 4.

- Вземете следното уравнение: aPCl5 + bH2O = cH3PO4 + dHCl. Беше заявено, че a = 1, което означава, че c = a, d = 5a и 2b = 3c + d. Извършени изчисления, c = 1, d = 5 и b = 4.


