Съдържание
По химия електроотрицателност тя е мярка за привличането, което един атом упражнява върху електроните в връзка. Атом с висока електроотрицателност привлича електрони с голяма интензивност, докато атом с ниска електроотрицателност ще го направи с малка интензивност. Тези стойности се използват за прогнозиране как ще се държат различни атоми, когато са свързани помежду си, което прави тази тема важно умение в основната химия.
стъпки
Метод 1 от 3: Основни понятия за електронегативност
Разберете, че химичните връзки се случват, когато атомите споделят електрони. За да разберете електронегативността, важно е първо да разберете какво е „връзка“. Казват, че всеки два атома в молекула, "свързани" един с друг в молекулна диаграма, имат връзка между тях. По същество това означава, че те споделят набор от два електрона - всеки атом допринася атом за връзката.
- Точните причини за това защо атомите споделят електрони и се свързват заедно не съответстват на фокуса на тази статия. Ако искате да научите повече, потърсете в интернет основните понятия за химически връзки.
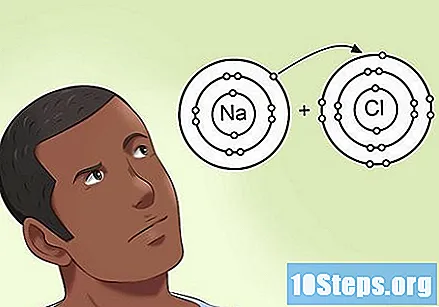
Разберете как електронегативността влияе на електроните, присъстващи в връзката. Когато два атома споделят набор от два електрона в една връзка, не винаги има еднакво споделяне между тях. Когато един от тях има по-висока електроотрицателност от атома, към който е прикрепен, той приближава двата електрона до себе си. Атом с много висока електроотрицателност може да изтегли електроните на своя страна във връзката, почти отменяйки споделянето с другия.- Например, в молекулата NaCl (натриев хлорид) хлорният атом има висока електроотрицателност, а натрият - ниска електроотрицателност. Скоро ще бъдат изтеглени електроните към хлора и далеч от натрий.

Използвайте таблицата за електроотрицателност като ориентир. Таблицата с електроотрицателност представя елементите, подредени точно като периодичната таблица, но с всеки атом, обозначен с неговата електроотрицателност. Те могат да бъдат намерени в няколко учебника по химия, в технически статии, а също и в интернет.- Ето една отлична таблица за електроотрицателност. Обърнете внимание, че тя използва скалата на електронегативността на Полинг, която е по-често срещана. Съществуват обаче и други начини за измерване на електроотрицателност, един от които ще бъде показан по-долу.
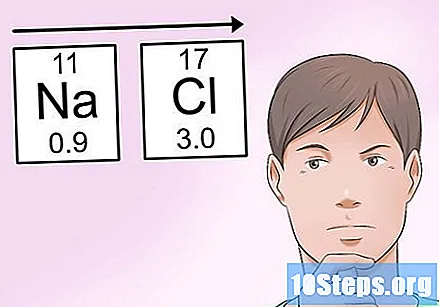
Запомнете тенденциите в електроотрицателността, за да правите оценки лесно. Ако нямате под ръка таблица с електроотрицателност, все още е възможно да оцените тази стойност въз основа на вашето местоположение в периодичната таблица. Като основно правило:- Електроотрицателността на един атом се увеличава докато преминете към прав в периодичната таблица.
- Електроотрицателността на един атом се увеличава докато се преместите към нагоре в периодичната таблица.
- Следователно атомите в горния десен ъгъл имат най-високите стойности на електроотрицателност, а тези в долния ляв ъгъл имат най-ниските.
- Например, в предишния пример за NaCl, можете да определите, че хлорът има по-висока електроотрицателност от натрия, тъй като е почти в най-високата дясна точка. От друга страна, натрият е далеч вляво от таблицата, което го прави един от най-малко ценните атоми.
Метод 2 от 3: Намиране на връзки с електроотрицателност
Намерете разликата в електроотрицателността между двата атома. Когато два атома са свързани заедно, разликата между техните стойности на електроотрицателност разкрива много за качеството на тази връзка. Извадете най-малката стойност от най-голямата, за да намерите разликата.
- Например, ако гледаме HF молекулата, ще извадим стойността на електроотрицателността на водорода (2.1) от тази на флуор (4.0). 4,0 - 2,1 = 1,9.
Ако разликата е под 0,5, връзката е ковалентна и неполярна. Тук електроните се споделят в почти еднаква степен. Тези връзки не образуват молекули с големи разлики в заряда в двата края. Полярните връзки често са много трудни за скъсване.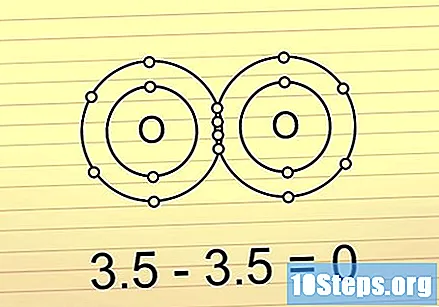
- Например молекулата О2 представя този тип връзка. Тъй като двете молекули кислород имат еднаква електроотрицателност, разликата между тях е равна на 0.
Ако разликата е между 0,5 и 1,6, връзката е ковалентна и полярна. Тези връзки държат повече електрони в единия край, отколкото в другия. Това прави молекулата малко по-отрицателна в края с повече електрони и малко по-положителна в края без тях. Дисбалансът на заряда в тези връзки позволява на молекулите да участват в някои специфични реакции.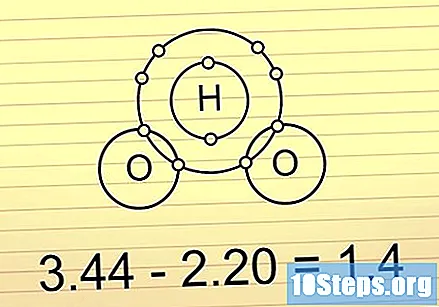
- Добър пример за това е Н молекулата2О (вода). О е по-електроотрицателен от два Н и следователно държи електроните по-близо и прави цялата молекула частично отрицателна в О-края и частично положителна в Н-краищата.
Ако разликата е по-голяма от 2, връзката е йонна. В тези връзки електроните са разположени изцяло в единия край. Най-електроотрицателният атом получава отрицателен заряд, а най-малко електроотрицателен атом придобива положителен заряд. Този тип връзка позволява на атомите да реагират с други атоми или освен това да бъдат разделени от полярни атоми.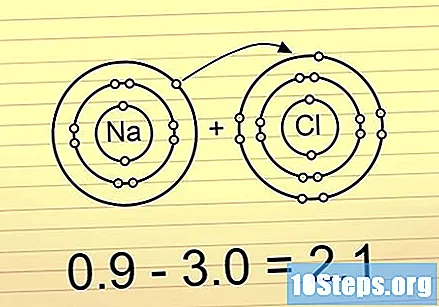
- Пример за това е NaCl (натриев хлорид). Хлорът е толкова електроотрицателен, че дърпа двата електрона от връзката един към друг, оставяйки натрий с положителен заряд.
Ако разликата е между 1.6 и 2, потърсете метал. ако там метал, присъстващ в връзката, това показва, че е така йонна, Ако има други неметали, връзката е полярна ковалентна.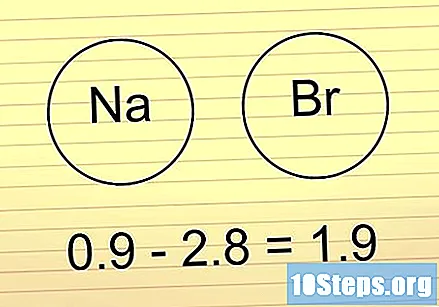
- Метали включват повечето от атомите вляво и в центъра на периодичната таблица. Тази страница има таблица, показваща кои елементи са метали.
- Нашият предишен HF пример попада в тази група. Тъй като H и F не са метали, връзката ще бъде полярна ковалентна.
Метод 3 от 3: Открийте електролигативността на Mulliken
Намерете първата йонизационна енергия на вашия атом. Електроотрицателността на Mulliken се състои от метод на измерване, малко по-различен от този, открит в таблицата на Pauling по-горе. За да намерите стойността му за даден атом, намерете първата си йонизационна енергия. Това е енергията, необходима, за да може атомът да освободи един единствен електрон.
- Тази стойност вероятно може да се намери в химическите референтни материали. Тази страница има добра таблица, която можете да използвате (превъртете надолу, за да я намерите).
- Като пример, нека кажем, че искате да разберете каква е електроотрицателността на лития (Li). В таблицата на страницата по-горе можем да видим, че първата йонизационна енергия е еквивалентна на 520 kJ / mol.
Разберете какъв е електронният афинитет на атома. Това е измерване на енергията, получена при добавяне на електрон към атома за образуване на отрицателен йон. Отново това е нещо, което трябва да се намери в референтните материали. Тази страница има ресурси, които могат да бъдат полезни.
- Електронният афинитет на лития е равен на 60 kJ mol.
Решете уравнението на електроотрицателността на Мъликен. Когато се използва kJ / mol като енергийна единица, уравнението на електроотрицателност на Mulliken може да бъде записано като ENMulliken = (1.97 × 10) (Eаз + Еи на) + 0,19, Поставете известните данни в уравнението и намерете стойността на ENMulliken.
- В нашия пример ще стигнем до следната резолюция:
- ENMulliken = (1.97 × 10) (Eаз + Еи на) + 0,19
- ENMulliken = (1,97 × 10)(520 + 60) + 0,19
- ENMulliken = 1,143 + 0,19 = 1,333
- В нашия пример ще стигнем до следната резолюция:
Съвети
- В допълнение към скалите Pauling и Mulliken има и други скали за електронегативност, като Allred-Rochow, Sanderson и Allen. Всеки от тях има свои собствени уравнения за изчисляване на електронегативността (а някои от тях могат да бъдат доста сложни).
- Електроотрицателност няма мерна единица.