
Съдържание
Въпреки че всички атоми на един и същ елемент съдържат един и същ брой протони, броят на неутроните може да варира. Знаейки колко неутрони има определен атом може да ви помогне да определите дали частицата е правилна в този елемент или изотоп, който ще има повече или по-малко неутрони. Определянето на броя на неутроните в един атом е доста просто и не изисква експеримент. За да изчислите броя на неутроните в обикновен атом или изотоп, следвайте тези инструкции с периодична таблица в ръка.
стъпки
Метод 1 от 2: Намиране на броя на неутралите в общ атом
Намерете елемента в периодичната таблица. За този пример, нека да разгледаме OS (Os), който е в шестия ред, отгоре надолу.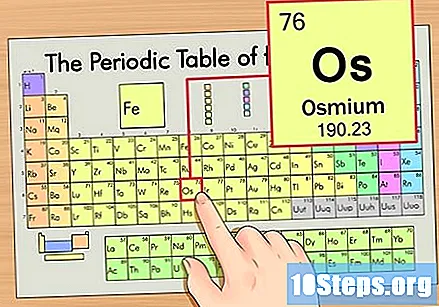
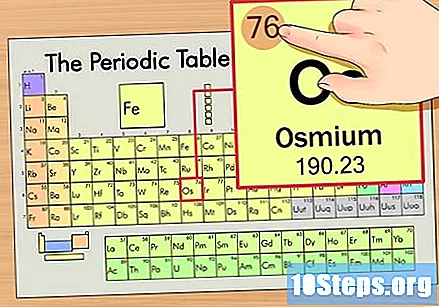
Намерете атомния номер на елемента. Това обикновено е най-видимото число за определен елемент и обикновено е над неговия символ (в таблицата, която използваме, всъщност няма друго число, посочено). Атомното число е броят на протоните в един атом на този елемент, Броят на Os е 76, което означава, че Osmium атом има 76 протона.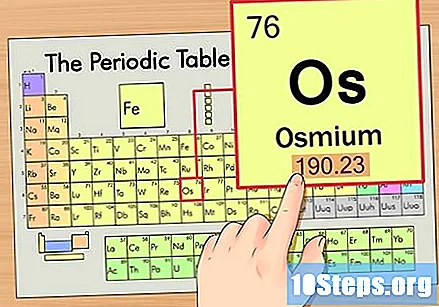
Намерете атомното тегло на елемента. Това число обикновено се намира под атомния символ. Обърнете внимание, че таблицата в този пример се основава само на атомното число и не изброява атомното тегло. Това не винаги ще бъде така. Осмиумът има атомно тегло 190,23.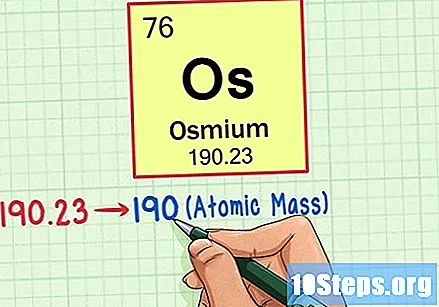
Закръглете атомната тежест до най-близкото цяло число, за да намерите атомната маса. В нашия пример 190,23 ще бъде закръглено до 190, което ще доведе до атомна маса от 190 за Осмия.- Атомната маса е средна стойност от изотопите на елемента. Следователно обикновено не е цяло число.
Извадете атомното число от атомната маса. Тъй като по-голямата част от масата на атома се намира в протоните и неутралите му, изваждането на броя на протоните (тоест атомното число) от атомната маса ще ви даде числото изчислява на неутроните в атома. Числото след десетичната запетая обикновено представлява много малка маса електрони в атома. В нашия пример това е: 190 (атомна маса) - 76 (брой протони) = 114 (брой неутрони).
Запомнете формулата. За да намерите броя на неутроните в бъдеще, просто използвайте тази формула: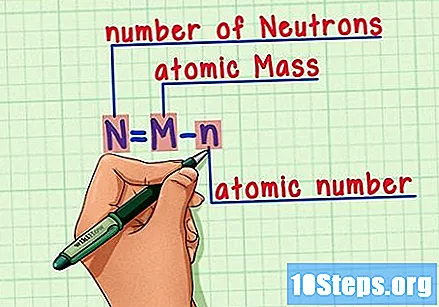
- N = M - n.
- N = брой на нeutrons.
- M = Матомно печено.
- n = натомен хамерус.
- N = M - n.
Метод 2 от 2: Намиране на броя на неутроните в изотоп
Намерете елемента в периодичната таблица. Например, нека използваме изотопа въглерод-14. Тъй като неизотопната форма на въглерод-14 е просто въглерод (С), намерете този елемент в периодичната таблица (във втория ред).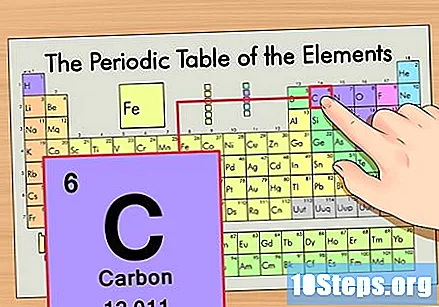
Намерете атомния номер на елемента. Това обикновено е най-видимото число за определен елемент и обикновено е над неговия символ (в таблицата, която използваме, всъщност няма друго число, посочено). Атомното число е броят на протоните в един атом на този елемент, С е число 6, което означава, че въглеродният атом има 6 протона.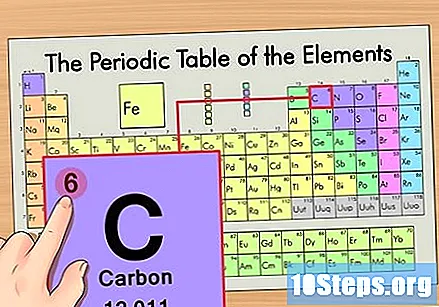
Намерете атомната маса. Това е невероятно лесно с изотопите, тъй като те са кръстени на тяхната атомна маса. Въглерод-14 има атомна маса 14. След като откриете атомната маса на изотопа, процесът за намиране на броя на неутроните е същият като този, използван за обикновените атоми.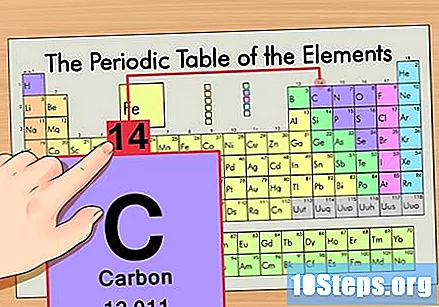
Извадете атомното число от атомната маса. Тъй като по-голямата част от масата на атома се намира в протоните и неутралите му, изваждането на броя на протоните (тоест атомното число) от атомната маса ще ви даде числото изчислява на неутроните в атома. Числото след десетичната запетая обикновено представлява много малка маса електрони в атома. В нашия пример това е: 14 (атомна маса) - 6 (брой протони) = 8 (брой неутрони).
Запомнете формулата. За да намерите броя на неутроните в бъдеще, просто използвайте тази формула: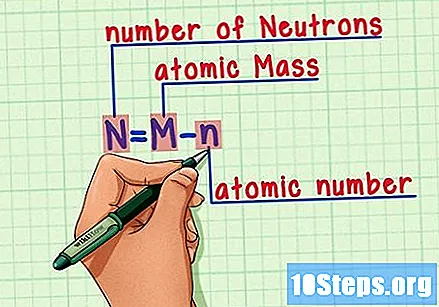
- N = M - n.
- N = брой на нeutrons.
- M = Матомно печено.
- n = натомен хамерус.
- N = M - n.
Съвети
- Osmium, твърд метал при стайна температура, получава името си от гръцката дума за „мирис“, „osme“.
- Протоните и неутроните съставляват почти цялото тегло на елементите, докато електроните и други разнообразни частици представляват нищожна маса (приближаваща се до нулева маса). Тъй като протонът е с еднаква тежест като неутрален и атомното число представлява броя на протоните, можем просто да извадим броя на протоните от общата маса.
- Ако не сте сигурни кое число е кое в периодичната таблица, просто не забравяйте, че то обикновено се прави около атомното число (тоест броят на протоните), което започва с 1 (Водород) и се увеличава с една единица на отляво надясно, завършващ в 118 (Ununóctio). Това е така, защото броят на протоните в един атом определя какъв е този атом, което улеснява организирането на елементарната характеристика (например, атом с 2 протона винаги ще бъде хелий, точно както друг атом със 79 протона винаги ще бъде Злато).


